Zasada działania baterii
Jak działa zegar ścienny, pilot do telewizora lub zabawka dla dzieci sterowana radiowo? Większość osób bez wahania odpowie „z baterii” i w zasadzie będzie miała rację. Jest jednak mało prawdopodobne, aby którykolwiek z nich był w stanie powiedzieć, jak dokładnie potrojona jest przenośna bateria, jak działa i bez czego cały proces przesyłania prądu elektrycznego z baterii do konsumenta końcowego byłby niemożliwy. Wypełnijmy tę irytującą lukę w wiedzy.
Zasada działania baterii
Aby zrozumieć zasadę działania konwencjonalnej baterii AA, trzeba mieć ogólne pojęcie o jej budowie. Tak więc każda bateria składa się z trzech głównych elementów - anody, katody i elektrolitu. Co więcej, te ostatnie mogą mieć praktycznie dowolny stan skupienia: katoda i anoda umieszczone w roztworze soli w zasadzie są także „baterią”, tylko w formie nietypowej dla przeciętnego człowieka.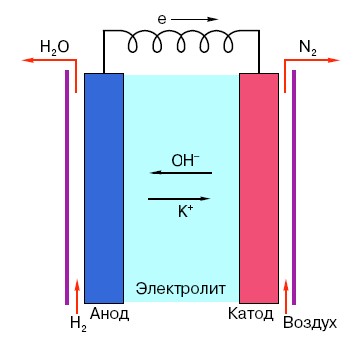
Ciekawy! Tak zwana „kolumna galwaniczna”, wynaleziona przez Alessandro Voltę, również zawierała wszystkie elementy niezbędne do wytwarzania prądu elektrycznego. Składała się z ułożonych jedna na drugiej płytek cynkowych i miedzianych, pomiędzy którymi jako „warstwa” umieszczono tkaninę nasączoną kwasem.
Anoda w takich układach jest głównym źródłem elektronów, które jak wiemy ze szkolnych zajęć z fizyki mają ładunek ujemny.Cząstki naładowane ujemnie przyciągają się do cząstek dodatnich i w tym przypadku powierzchnia katody działa jak „plus”.
Ale to nie wystarczy, aby pojawił się prąd elektryczny, ponieważ elektrony potrzebują również swego rodzaju „autostrady” - ośrodka, który wspierałby oddziaływanie katody i anody. To tutaj „na scenie” pojawia się elektrolit – sól, zasada lub kwas zdolny do przewodzenia prądu.
Przyjrzyjmy się zasadzie działania na konkretnym przykładzie: istnieje akumulator o napięciu 18 woltów. Napięcie między znajdującymi się w nim elektrodami jest stabilne do momentu podłączenia go do sieci. Gdy tylko pojawi się konsument (na przykład zwykła żarówka), napięcie zaczyna stopniowo spadać, prąd zaczyna płynąć z elektrody „ujemnej” do „dodatniej”, a w elektrolicie zachodzi reakcja chemiczna mająca na celu utrzymując różnicę potencjałów pomiędzy elektrodami.
Odniesienie. Im więcej energii potrzebuje konsument, tym intensywniejsza jest reakcja wewnątrz akumulatora i tym szybciej ulegnie on awarii.
Jak działa akumulator, czym różni się od zwykłego
Przyjrzeliśmy się więc klasycznym akumulatorom „palcowym” i „małym palcem” i wiemy, że żywotność większości z nich jest ściśle ograniczona (niezależnie od tego, co mówią znani producenci). Co jednak z tzw. akumulatorami – akumulatorami typu akumulatorowego, które w procesie reakcji potrafią nie tylko zużywać energię, ale także ją akumulować i przechowywać przez długi czas?
Aby zrozumieć zasadę działania baterii, należy sięgnąć do chemii. Weźmy za przykład... Zwykłe ognisko na węgiel drzewny.Nieważne, jak pięknie i fascynująco wygląda płomień, każdy obserwujący go chemik wie, że proces ten jest po prostu długotrwałą reakcją utleniania paliwa. Podczas spalania węgla wchodzi w interakcję z tlenem i w wyniku tej reakcji otrzymujemy:
- dwutlenek węgla;
- światło;
- ciepły.
A jeśli te dwa ostatnie punkty są w stanie ogrzać duszę i ciało, to nie możemy w żaden sposób wykorzystać dwutlenku węgla, ponieważ jest to produkt uboczny reakcji, czyli tak naprawdę jego odpad. Reakcja utleniania kończy się, gdy wyczerpią się pierwiastki wyjściowe: tlen i węgiel. Zatrzymanie reakcji w akumulatorze następuje dokładnie w ten sam sposób, gdy substancje wyjściowe zostaną całkowicie wyczerpane i zostaną jedynie „odpady”.
W akumulatorze wszystko dzieje się trochę inaczej. Faktem jest, że zachodząca w nim reakcja należy do kategorii odwracalnej, to znaczy w pewnych warunkach można ją „odwrócić”, przywracając wszystkie substancje do ich pierwotnego stanu. To właśnie możliwość zajścia odwracalnej reakcji w akumulatorze umożliwia jego ładowanie.
W akumulatorze podłączonym do sieci reakcja przebiega w przeciwnym kierunku, a prąd płynie od „plusa” do „minusu”, a nie odwrotnie. W rezultacie produkt reakcji tworzy substancje wyjściowe, a właściciel akumulatora otrzymuje dostępną „odzyskaną” energię w przenośnym formacie. To wszystko!





